对化学物质分类的方法(对化学物质分类的方法)
1.对化学物质分类的方法有哪些
1、物质分类的方法:
根据纯净物的颜色、状态、气味、溶解性、可燃性及组成等对物质进行分
类。
如对下列七种物质:氯化钠、硫酸、氧气、醋酸、氯气、氧化镁、高锰酸
钾,根据分类标准不同可以有不同的分类结果:
按颜色分类:
白色:氯化钠、氧化镁
无色:硫酸、氧气、醋酸
黄绿色:氯气
紫黑色:高锰酸钾
按状态分类
固态:氯化钠、氧化镁、高锰酸钾
液态:硫酸、醋酸
气态:氧气、氯气
按组成分类
单质:氧气、氯气
化合物:高锰酸钾、氧化镁、氯化钠、硫酸、醋酸
按气味分类
有气味的物质:氯气、醋酸
无气味的物质:氧气、高锰酸钾、氧化镁、氯化钠、硫酸
2、单质和化合物:
(1)单质的概念:单质是由同种元素组成的纯净物。
说明:
①单质必须是纯净物,两者是从属关系,即单质概念小,纯净物概念大。
②单质必须是由同一种元素组成。
③一种元素可以组成多种单质,如氧气(O2)和臭氧(O3),两者混在一起不是单质而是混合物,除此之外还有红磷和白磷、金刚石和石墨等。
④单质的分类:
根据单质的性质不同,单质可分为金属单质和非金属单质。
(2)化合物的概念:化合物是由不同种元素组成的纯净物
3、氧化物:
(1)概念:由两种元素组成,其中一种是氧元素的化合物称为氧化物。
(2)分类:根据氧化物的组成,除去氧元素,另一种元素是金属元素的氧化物称为金属氧化物,如FeO、CuO等;另一种元素是非金属元素的氧化物称为非金属氧化物,如CO、CO2、SO2、H2O等。
4、无机化合物和有机化合物:
(1)无机化合物
无机化合物一般指由碳以外的其他元素组成的化合物,如NaCl、KClO3、H2O等,也包括少数的含碳化合物,如CO、CO2、CaCO3等。
(2)有机化合物
有机化合物主要是指含碳的化合物(碳的氧化物、碳酸、碳酸盐除外),如酒精、蔗糖等。
(3)有机化合物的性质
有机化合物具有相似的性质,如:具有可燃性,完全燃烧时一般生成二氧化碳和水;不完全燃烧时有炭黑小颗粒(黑烟成分)产生。
(4)有机化合物和无机化合物的区别
无机物一般能溶于水,溶液能导电,而大多数有机物都难溶于水,熔点低,受热易分解,容易燃烧,不易导电等。
2.物质分类的方法有哪些
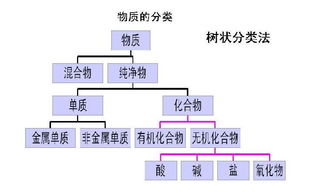
物质的分类bai的分类的方法有三种:1、单一分类法对对象使用一种标准的分类法(如氧化物按组成元素分为金属氧化物、非金属氧化物)2、交叉分类法对对象用多种不同的单一分类法进行分类(如将H2SO4按是否有du氧元素、酸的强弱、酸的元数等不同标准进行分类,H2SO4分别属于含氧酸、zhi强酸和二元酸)3、树状分类法根据被分对象的整体与分支的类型之间的关系,以陈列式的形状(树)来定义。
具体如下:1、根据有无固定组成dao分为 纯净物、混合物;2、根据元素组成分为 化合物、单质;3、根据在水溶液或熔化状态能否导电分为 电解回质、非电解质;4、根据分散物质颗粒大小,将混合物分为 溶液、悬浊液、乳浊液、胶体;5、根据是否含碳元素,将化合物分为 有机物、无机物;6、根据化学答键类型,将化合物分为 离子化合物、共价化合物;7、根据在氧化还原反应中的表现,将反应物分为 氧化剂、还原剂。
3.化学的物质分类怎么分
由同种元素组成的纯净物叫做单质,
由不同种元素组成的纯净物叫做化合物,
由两种元素组成,且其中一种元素是氧元素的化合物叫做氧化物,
汽油、煤油、酒精、蔗糖、脂肪、蛋白质等等含碳化合物叫做有机物,
一般把不含碳的化合物叫做无机物,一氧化碳、二氧化碳、碳酸、碳酸盐等少数含碳化合物,由于它们的组成和性质跟无机物一致,把他们归入无机物来进行研究。
把电离时生成的阳离子全部事情离子的化合物叫做酸。(由氢元素和酸根组成的化合物叫做酸)
由金属元素和氢氧根组成的化合物叫做碱。
由金属元素(或铵根)组成的化合物叫做
4.化学物质的分类
一.纯净物
1.单质 :金属单质和非金属单质。
金属单质主要有:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、Hg、Ag、Au等
非金属单质主要有:C、S、P、Si、O、N、H、Cl、He、Ne、Ar
2.化合物:有机物:烃、烃(烃的衍生物)、营养物质
无机物:氧化物、氢化物、酸、碱和盐等
烃:烷烃(甲烷),烯烃(乙烯)
营养物质:葡萄糖、蛋白质、脂质[1]
氧化物:含有氧元素的化合物(无机物)
酸性氧化物:SO2、CO2、P2O5、Mn2O7等
碱性氧化物:MgO、CaO、Na2O(一定是金属氧化物)等
两性氧化物:Al2O3、ZnO等
不成盐氧化物:CO、NO等
过氧化物:Na2O2、H2O2等
酸:指电离时产生的阳离子全部都是氢离子的化合物
含氧酸:HNO3等
无氧酸:HCl等
一元酸:HCl、H2S等
二元酸:H2CO3、H2SO4、H2S等
多元酸:H3PO4等
碱:指电离时产生的阴离子全部都是氢氧根离子的化合物
强碱:NaOH等
弱碱:Fe(OH)3等
可溶性碱:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O
不溶性碱:Mg(OH)2、Cu(OH)2等
盐:指电离时生成金属阳离子(或NH4)和酸根离子的化合物
正盐:Na2CO3、NaCl、BaSO4等
酸式盐:NaHCO3等
碱式盐:Cu2(OH)2CO3等
复盐:KAl(SO4)2·12H2O
二.混合物:溶液、胶体、悬浊液、乳浊液等
声明:本网站尊重并保护知识产权,根据《信息网络传播权保护条例》,如果我们转载的作品侵犯了您的权利,请在一个月内通知我们,我们会及时删除。
蜀ICP备2020033479号-4 Copyright © 2016 学习鸟. 页面生成时间:2.878秒








